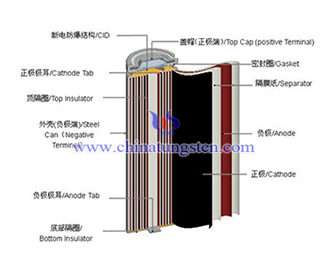
니켈 수소 전지(NiH Battery)

프로필
니켈 수소 배 터 리 는 친 환경 배터리 로 카드뮴 을 함유 하지 않 는 다.이 배 터 리 는 니켈, 카드뮴 배 터 리 를 개량 하여 카드뮴 을 수소 흡수 할 수 있 는 금속 니켈 로 대체 하여 환경 보호 와 더 큰 전 용량 (용량 2900 mAh) 을 실현 하 는 목적 이다.
성능
니켈 카드뮴 배터리 보다 친 환경 적 이 고 용량 이 크다.
리튬 배터리 보다 자체 방전 반응 이 높다.
탄소 나 알칼리성 전지 에 비해 더 큰 출력 배 터 리 를 갖 고 있다.
화학 원리
배터리 충전 시 수소 산화칼륨 (KOH) 전해 액 에서 수소 이온 (H +) 이 방출 되 고 이 화합물 들 이 흡수 되 어 수소 가스 (H2) 가 생기 지 않도록 배터리 내부 의 압력 과 체적 을 유지한다.배터리 가 방전 되면 이 수소 이온 들 은 상 반 된 과정 을 거 쳐 원래 있 던 곳 으로 돌아간다.
특성
전압 = 1.2V
에너지 / 체중 = 30-80 Wh/kg (와트시 / 킬로그램) 即 108-880kJ/kg (천 줄 의 버섯/킬로그램)
에너지∕부피 = 140-300 Wh/L (瓦특별 시간 / 리터) 即 504-1188kJ/kg (천 줄 의 버섯/千克)
자체 방전 율 = 보통 매월 30%, 낮은 자체 방전 모델 은 매년 15 - 30% 이다
충전 충전 순환 횟수 = 500 - 1000 회
니켈 수소 배 터 리 는 수소 이온 과 금속 니켈 로 합성 되 고 전력 예비 액 은 니켈, 카드뮴 배터리 보다 30% 더 많 으 며 사용 수명 도 더 길 고 환경 에 오염 이 없다.니 하 드 건전 지 는 가격 이 니 카드뮴 배터리 보다 훨씬 비 싸 고, 리튬 배터리 보다 성능 이 떨어진다 는 단점 이 있다.
화학 성분
니켈 수소 전지 중의 금속 부분 은 실제로는 금속 호화물 이다.많은 종류의 금속 은 니켈 전지 제조 에 사용 되 었 다. 이들 은 주로 두 가지 로 나 뉘 는데 가장 흔히 볼 수 있 는 것 은 AB5 종류 이다. A 는 희토 류 원소 의 혼합물 (또는) 에 티타늄 (Ti) 을 첨가 하고 B 는 니켈 (Ni), 코발트 (Co), 망간 (MN), (또는), 알루미늄 (Al) 등 이다.한편, 일부 고 용량 배터리 의 '여러 가지 성분 을 포함 하 는' 전극 은 AB2 로 구성 되 는데 여기 있 는 A 는 티타늄 (Ti) 또는 바나듐 (V) 이 고 B 는 지르코늄 (Zr) 또는 니켈 (Ni) 이 고 크롬 (Cr), 코발트 (Co), 철 (Feel) 과 (또는) 망간 (MN) 이 있다.모든 이러한 화합물 은 같은 역할 을 하 는데 그것 이 역 동적 으로 금속 성 수산화물 을 형성 하 는 것 이다.배터리 충전 시 수소 산화칼륨 (KOH) 전해 액 에서 수소 이온 (H +) 이 방출 되 고 이 화합물 들 이 흡수 되 어 수소 가스 (H2) 가 생기 지 않도록 배터리 내부 의 압력 과 체적 을 유지한다.배터리 가 방전 되면 이 수소 이온 들 은 상 반 된 과정 을 거 쳐 원래 있 던 곳 으로 돌아간다.
전기화학 원리
KOH 작 전해 액 (전해질 7moL / LKOH + 15g / LIOH)
충전 때
양극 반응: Ni(OH)2 + OH- → NiOOH + H2O + e-
음극 반응: M + H2O + e- → MH + OH-
총 반응: M + Ni(OH)2 → MH + NiOOH
방전 시
正极:NiOOH + H2O + e- → Ni(OH)2 + OH-
음극: MH + OH- → M + H2O + e-
총 반응: MH + NiOOH → M + Ni(OH)2
이상 식 에서 M 은 수소 합금 이 고 MH 는 수소 원 자 를 흡수 하 는 수소 합금 이 며 가장 많이 사용 되 는 수소 합금 은 LaNi5 이다.
3TG 무 갈등 광산 성명 서
3TG 무 충돌 광산 성명 서 를 클릭 하여 다운로드 받 을 수 있 습 니 다.
그림
니켈 수소 전지 에 관 한 더 많은 그림 은 중텅스텐 사진 망 을 방문 할 수 있다.
시장가 격
매일 가격 은 중텅스텐 온라인 공인 의 "중텅스텐 온라인" 또는 가격 웹 사 이 트 를 방문 할 수 있다.